LAS PROTEINAS
Las proteínas o prótidos son moléculas formadas por cadenas lineales de aminoácidos. El término proteína proviene de la palabra francesa protéine y ésta del griego πρωτεῖος (proteios), que significa 'prominente, de primera calidad'.
Por sus propiedades físico-químicas, las proteínas se pueden clasificar en proteínas simples (holoproteidos), que por hidrólisis dan solo aminoácidos o sus derivados; proteínas conjugadas (heteroproteidos), que por hidrólisis dan aminoácidos acompañados de sustancias diversas, y proteínas derivadas, sustancias formadas por desnaturalización
y desdoblamiento de las anteriores. Las proteínas son necesarias para
la vida, sobre todo por su función plástica (constituyen el 80% del protoplasma deshidratado de toda célula), pero también por sus funciones biorreguladoras (forman parte de las enzimas) y de defensa (los anticuerpos son proteínas).
Las proteínas desempeñan un papel fundamental para la vida y son las biomoléculas más versátiles y diversas. Son imprescindibles para el crecimiento del organismo y realizan una enorme cantidad de funciones diferentes, entre las que destacan:
- Estructural. Esta es la función más importante de una proteína (Ej: colágeno)
- Inmunológica (anticuerpos)
- Enzimática (Ej: sacarasa y pepsina)
- Contráctil (actina y miosina)
- Homeostática: colaboran en el mantenimiento del pH (ya que actúan como un tampón químico)
- Transducción de señales (Ej: rodopsina)
- Protectora o defensiva (Ej: trombina y fibrinógeno)
Las proteínas están formadas por aminoácidos.
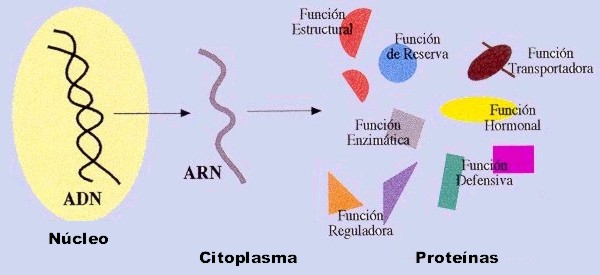
Las proteínas de todos los seres vivos están determinadas mayoritariamente por su genética (con excepción de algunos péptidos antimicrobianos de síntesis no ribosomal), es decir, la información genética determina en gran medida qué proteínas tiene una célula, un tejido y un organismo.
Las proteínas se sintetizan dependiendo de cómo se encuentren regulados los genes
que las codifican. Por lo tanto, son susceptibles a señales o factores
externos. El conjunto de las proteínas expresadas en una circunstancia
determinada es denominado proteoma.

Clasificación
Según su forma
-
- Globulares: se caracterizan por doblar sus cadenas en una forma esférica apretada o compacta dejando grupos hidrófobos hacia adentro de la proteína y grupos hidrófilos hacia afuera, lo que hace que sean solubles en disolventes polares como el agua. La mayoría de las enzimas, anticuerpos, algunas hormonas y proteínas de transporte, son ejemplos de proteínas globulares.
-
- Mixtas: posee una parte fibrilar (comúnmente en el centro de la proteína) y otra parte globular (en los extremos).

Según su composición química
-
- Simples: su hidrólisis sólo produce aminoácidos. Ejemplos de estas son la insulina y el colágeno (globulares y fibrosas). A su vez, las proteínas se clasifican en:
- a) Escleroproteínas: Son esencialmente insolubles, fibrosas, con un grado de cristalinidad relativamente alto. Son resistentes a la acción de muchas enzimas y desempeñan funciones estructurales en el reino animal. Los colágenos constituyen el principal agente de unión en el hueso, el cartílago y el tejido conectivo. Otros ejemplos son la queratina, la fibroína y la sericina.
- b) Esferoproteínas: Contienen moléculas de forma más o menos esférica. Se subdividen en cinco clases según sus solubilidad:
- I.-Albúminas: Solubles en agua y soluciones salinas diluidas. Ejemplos: la ovoalbúmina y la lactalbúmina.
- II.-Globulinas: Insolubles en agua pero solubles en soluciones salinas. Ejemplos: miosina, inmunoglobulinas, lactoglobulinas, glicinina y araquina.
- III.- Glutelinas: Insolubles en agua o soluciones salinas, pero solubles en medios ácidos o básicos. Ejemplos: oricenina y las glutelinas del trigo.
- IV.- Prolaminas: Solubles en etanol al 50%-80%. Ejemplos: gliadina del trigo y zeína del maíz.
- V.- Histonas son solubles en medios ácidos.
- Conjugadas o heteroproteínas: su hidrólisis produce aminoácidos y otras sustancias no proteicas con un grupo prostético.
NIVELES DE ORGANIZACIÓN ESTRUCTURAL DE LAS PROTEINAS
La
organización de una proteína viene definida por cuatro niveles estructurales
denominados: estructura primaria,
estructura secundaria, estructura terciaria y estructura cuaternaria. Cada una de estas estructuras informa de la
disposición de la anterior en el espacio.
Estructura
primaria es la secuencia
de aminoácidos de la proteína. Nos indica qué aminoácidos componen la cadena
polipeptídica y el orden en que dichos aminoácidos se encuentran. La función de
una proteína depende de su secuencia y de la forma que ésta adopte.
Estructura secundaria es la disposición de la secuencia de aminoácidos en el
espacio. Los aminoácidos, a medida que van siendo enlazados durante la síntesis
de proteínas y gracias a la capacidad de giro de sus enlaces, adquieren una
disposición espacial estable, la estructura
secundaria en donde la cadena se va enrollando en espiral:
La a(alfa)-hélice.
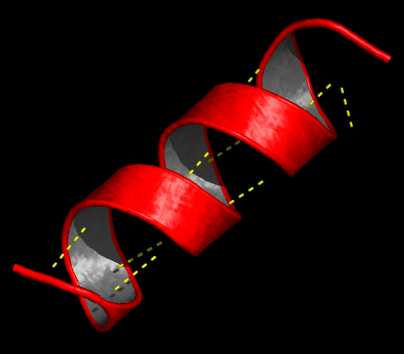
Esta
estructura se forma al enrollarse helicoidalmente sobre sí misma la estructura
primaria.
Se
debe a la formación de enlaces de hidrógeno entre el -C=O de un aminoácido y el
-NH- del cuarto aminoácido que le sigue.
La conformación beta.

En
esta disposición los aminoácidos no forman una hélice sino una cadena en forma
de zigzag, denominada disposición en lámina plegada.
Presentan
esta estructura secundaria la queratina de la seda o fibroína.
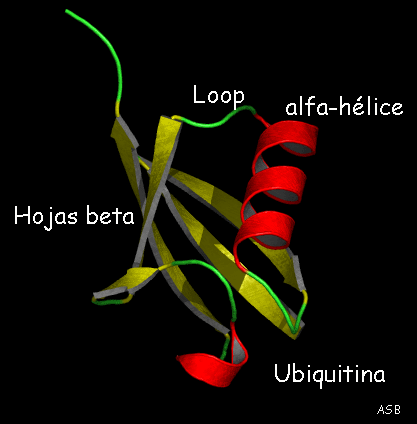
Estructura terciaria
informa sobre la disposición de la estructura secundaria
de un polipéptido al plegarse sobre sí misma originando una conformación
globular.
En
definitiva, es la estructura primaria la que determina cuál será la secundaria
y por tanto la terciaria.
Esta
conformación globular facilita la solubilidad
en agua y así realizar funciones de transporte,
enzimáticas, hormonales, etc.
Esta
conformación globular se mantiene estable gracias a la existencia de enlaces
entre los radicales R de los
aminoácidos. Aparecen varios tipos de enlaces:
1.-
el puente disulfuro entre los
radicales de aminoácidos que tienen azufre.
2.-
los puentes de hidrógeno.
3.-
los puentes eléctricos. (covalentes)
4.-
las interacciones hidrófobas.
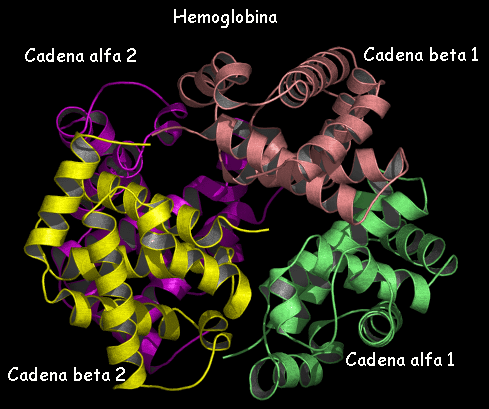
Estructura cuaternaria
informa de la unión, mediante enlaces débiles (no covalentes) de
varias cadenas polipeptídicas con estructura terciaria, para formar un complejo
proteico. Cada una de estas cadenas polipeptídicas recibe el nombre de protómero.
El
número de protómeros varía desde dos, como en la hexoquinasa; cuatro, como en la hemoglobina, o muchos, como la cápsida del virus de la
poliomielitis, que consta de sesenta unidades proteicas.
Funciones
Las proteínas ocupan un lugar de máxima importancia entre las moléculas constituyentes de los seres vivos (biomoléculas).
Prácticamente todos los procesos biológicos dependen de la presencia o
la actividad de este tipo de moléculas. Bastan algunos ejemplos para dar
idea de la variedad y trascendencia de las funciones que desempeñan.
Son proteínas:
- Casi todas las enzimas, catalizadores de reacciones químicas en organismos vivientes;
- Muchas hormonas, reguladores de actividades celulares;
- La hemoglobina y otras moléculas con funciones de transporte en la sangre;
- Los anticuerpos, encargados de acciones de defensa natural contra infecciones o agentes patógenos;
- Los receptores de las células, a los cuales se fijan moléculas capaces de desencadenar una respuesta determinada;
- La actina y la miosina, responsables finales del acortamiento del músculo durante la contracción;
- El colágeno, integrante de fibras altamente resistentes en tejidos de sostén.
Funciones de reserva. Como la ovoalbúmina en el huevo, o la caseína de la leche.
Todas las proteínas realizan elementales funciones para la vida celular, pero además cada una de éstas cuenta con una función más específica de cara a nuestro organismo.
Debido a sus funciones, se pueden clasificar en:
- 1. Catálisis: Está formado por enzimas proteicas que se encargan de realizar reacciones químicas de una manera más rápida y eficiente. Procesos que resultan de suma importancia para el organismo. Por ejemplo la pepsina, ésta enzima se encuentra en el sistema digestivo y se encarga de degradar los alimentos.
- 2. Reguladoras: Las hormonas son un tipo de proteínas las cuales ayudan a que exista un equilibrio entre las funciones que realiza el cuerpo. Tal es el caso de la insulina que se encarga de regular la glucosa que se encuentra en la sangre.
- 3. Estructural: Este tipo de proteínas tienen la función de dar resistencia y elasticidad que permite formar tejidos así como la de dar soporte a otras estructuras. Este es el caso de la tubulina que se encuentra en el citoesqueleto.
- 4. Defensiva: Son las encargadas de defender al organismo. Glicoproteínas que se encargan de producir inmunoglobulinas que defienden al organismo contra cuerpos extraños, o la queratina que protege la piel, así como el fibrinógeno y protrombina que forman coágulos.
- 5. Transporte: La función de estas proteínas es llevar sustancias a través del organismo a donde sean requeridas. Proteínas como la hemoglobina que lleva el oxígeno por medio de la sangre.
- 6. Receptoras: Este tipo de proteínas se encuentran en la membrana celular y llevan a cabo la función de recibir señales para que la célula pueda realizar su función, como acetilcolina que recibe señales para producir la contracción.
Propiedades de las proteínas
- Solubilidad: Se mantiene siempre y cuando los enlaces fuertes y débiles estén presentes. Si se aumenta la temperatura y el pH se pierde la solubilidad.
- Capacidad electrolítica: Se determina a través de la electroforesis, técnica analítica en la cual si las proteínas se trasladan al polo positivo es porque su molécula tiene carga negativa y viceversa.
- Especificidad: Cada proteína tiene una función específica que está determinada por su estructura primaria.
- Amortiguador de pH (conocido como efecto tampón): Actúan como amortiguadores de pH debido a su carácter anfótero, es decir, pueden comportarse como ácidos (donando electrones) o como bases (aceptando electrones).
Nutrición
Fuentes de proteínas
Las fuentes dietéticas de proteínas incluyen carne, huevos,
legumbres, frutos secos, cereales, verduras y productos lácteos tales
como queso o yogur. Tanto las fuentes proteínas animales como las vegetales poseen los 20 aminoácidos necesarios para la alimentación humana.
Calidad proteica
Las diferentes proteínas tienen diferentes niveles de familia
biológica para el cuerpo humano. Muchos alimentos han sido introducidos
para medir la tasa de utilización y retención de proteínas en humanos.
Éstos incluyen valor biológico, NPU (Net Protein Utilization), NPR
(Cociente Proteico Neto) y PDCAAS (Protein Digestibility Corrected Amino
Acids Score), la cual fue desarrollado por la FDA mejorando el PER
(Protein Efficiency Ratio). Estos métodos examinan qué proteínas son más
eficientemente usadas por el organismo. En general, éstos concluyeron
que las proteínas animales que contienen todos los aminoácidos
esenciales (leche, huevos, carne) y la proteína de soya son las más valiosas para el organismo.
Reacciones de reconocimiento
El reactivo de Biuret está formado por una disolución de sulfato de cobre en medio alcalino, este reconoce el enlace peptídico de las proteínas mediante la formación de un complejo de coordinación entre los iones Cu2+ y los pares de electrones no compartidos del nitrógeno que forma parte de los enlaces peptídicos, lo que produce una coloración rojo-violeta.
Se pone de manifiesto por la formación de un precipitado negruzco de
sulfuro de plomo. Se basa esta reacción en la separación mediante un
álcali, del azufre de los aminoácidos, el cual al reaccionar con una
solución de acetato de plomo, forma el sulfuro de plomo.
Reconoce residuos fenólicos, o sea aquellas proteínas que contengan tirosina.
Las proteínas se precipitan por acción de los ácidos inorgánicos
fuertes del reactivo, dando un precipitado blanco que se vuelve
gradualmente rojo al calentar.
Reconoce grupos aromáticos, o sea aquellas proteínas que contengan tirosina o fenilalanina, con las cuales el ácido nítrico forma compuestos nitrados amarillos.
Deficiencia de proteínas
Deficiencia de proteínas en países en vías de desarrollo.
La deficiencia de proteína es una causa importante de enfermedad y muerte en el tercer mundo. La deficiencia de proteína juega una parte en la enfermedad conocida como kwashiorkor. La guerra, la hambruna, la sobrepoblación y otros factores incrementaron la tasa de malnutrición y deficiencia de proteínas. La deficiencia de proteína puede conducir a una inteligencia reducida o retardo mental.
La malnutrición proteico calórica afecta a 500 millones de personas y
más de 10 millones anualmente. En casos severos el número de células blancas disminuye, de la misma manera se ve reducida drásticamente la habilidad de los leucocitos de combatir una infección.
Deficiencia de proteínas en países desarrollados La
deficiencia de proteínas es rara en países desarrollados pero un pequeño
número de personas tiene dificultad para obtener suficiente proteína
debido a la pobreza. La deficiencia de proteína también puede ocurrir en
países desarrollados en personas que están haciendo dieta para perder
peso, o en adultos mayores quienes pueden tener una dieta pobre. Las
personas convalecientes, recuperándose de cirugía, trauma o enfermedades
pueden tener déficit proteico si no incrementan su consumo para
soportar el incremento en sus necesidades. Una deficiencia también puede
ocurrir si la proteína consumida por una persona está incompleta y
falla en proveer todos los aminoácidos esenciales.
Exceso de consumo de proteínas
Como el organismo es incapaz de almacenar las proteínas, el exceso de proteínas es digerido y convertido en azúcares o ácidos grasos. El hígado retira el nitrógeno de los aminoácidos, una manera de que éstos pueden ser consumidos como combustible, y el nitrógeno es incorporado en la urea,
la sustancia que es excretada por los riñones. Estos órganos
normalmente pueden lidiar con cualquier sobrecarga adicional, pero si
existe enfermedad renal, una disminución en la proteína frecuentemente
será prescrita.
El exceso en el consumo de proteínas también puede causar la pérdida de calcio
corporal, lo cual puede conducir a pérdida de masa ósea a largo plazo.
Sin embargo, varios suplementos proteicos vienen suplementados con
diferentes cantidades de calcio por ración, de manera que pueden contrarrestar el efecto de la pérdida de calcio.
Algunos sospechan que el consumo excesivo de proteínas está ligado a varios problemas:
- Hiperactividad del sistema inmune.
- Disfunción hepática debido a incremento de residuos tóxicos.
- Pérdida de densidad ósea; la fragilidad de los huesos se debe a que el calcio y la glutamina se filtran de los huesos y el tejido muscular para balancear el incremento en la ingesta de ácidos a partir de la dieta. Este efecto no está presente si el consumo de minerales alcalinos (a partir de frutas y vegetales [los cereales son ácidos como las proteínas; las grasas son neutrales]) es alto.
En tales casos, el consumo de proteínas es anabólico para el hueso. Algunos investigadores piensan que un consumo excesivo de proteínas produce un incremento forzado en la excreción
del calcio. Si hay consumo excesivo de proteínas, se piensa que un
consumo regular de calcio sería capaz de estabilizar, o inclusive
incrementar, la captación de calcio por el intestino delgado, lo cual sería más beneficioso en mujeres mayores.
Las proteínas son frecuentemente causa de alergias y reacciones alérgicas a ciertos alimentos.
Esto ocurre porque la estructura de cada forma de proteína es
ligeramente diferente. Algunas pueden desencadenar una respuesta a
partir del sistema inmune, mientras que otras permanecen perfectamente
seguras. Muchas personas son alérgicas a la caseína (la proteína en la leche), al gluten (la proteína en el trigo) y otros granos, a la proteína particular encontrada en el maní o aquellas encontradas en mariscos y otras comidas marinas.
Es extremadamente inusual que una misma persona reaccione
adversamente a más de dos tipos diferentes de proteínas, debido a la
diversidad entre los tipos de proteínas o aminoácidos. Aparte de eso, las proteínas ayudan a la formación de la masa muscular.

No hay comentarios:
Publicar un comentario